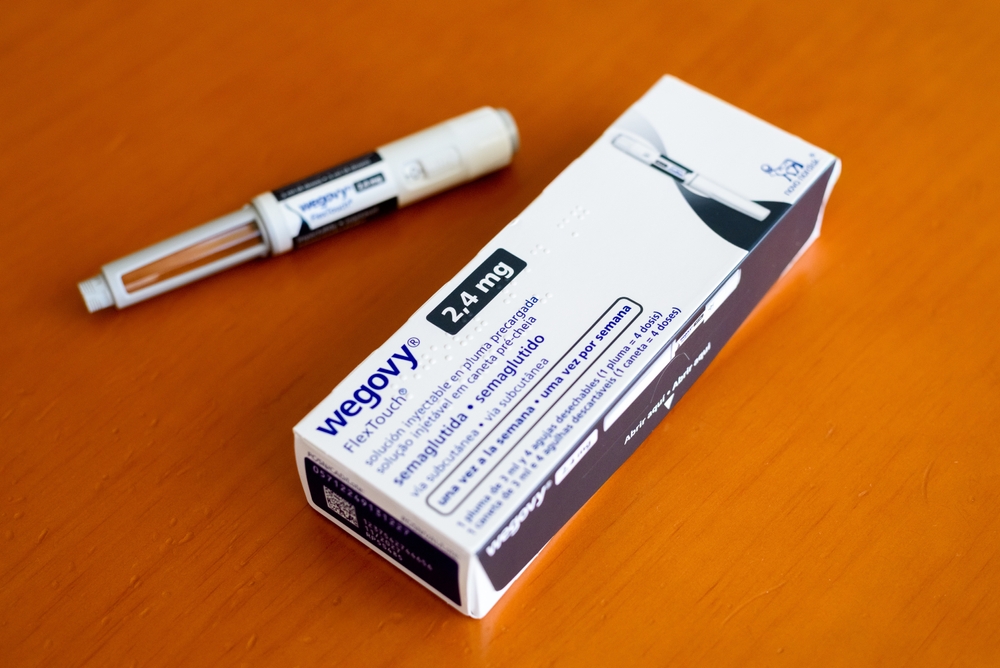
De populære legemidlene Ozempic og Wegovy diskuteres igjen.
Akkurat nå leser andre
Den danske legemiddelgiganten Novo Nordisk har mottatt et advarselsbrev fra det amerikanske mat- og legemiddeltilsynet, FDA.
Brevet gjelder selskapets prosedyrer for rapportering av mulige bivirkninger av legemidler med virkestoffet semaglutid.
Dette melder det amerikanske mediet CBS News.
Semaglutid er blant annet den aktive ingrediensen i Novo Nordisks diabetesmedisin Ozempic og vektreduksjonsmedisinen Wegovy, som de siste årene har vært blant selskapets mest suksessrike produkter.
Tre dødsfall nevnt i brevet
I advarselsbrevet, datert 5. mars, viser FDA til tre dødsfall blant pasienter som har blitt behandlet med medisiner som inneholder semaglutid.
Les også
I ett av tilfellene var det snakk om selvmord, mens det i et annet tilfelle ble rapportert om selvmordstanker hos en pasient.
FDA understreker imidlertid at myndigheten ikke konkluderer med at dødsfallene eller de psykologiske symptomene skyldes bruken av legemidlene.
Saken handler i stedet om hvorvidt Novo Nordisk har overholdt reglene for korrekt og rettidig rapportering av potensielle bivirkninger som kan være forbundet med medisinen.
Dette skriver Ekstrabladet.
Problemer oppdaget under inspeksjon
Ifølge CBS News ble problemene oppdaget under en inspeksjon ved Novo Nordisks amerikanske hovedkvarter i Plainsboro, New Jersey, tidlig i 2025.
Les også
FDA-inspektører fant forhold som ifølge myndigheten kunne tyde på manglende overholdelse av kravene til rapportering av bivirkninger.
Novo Nordisk bekrefter i en pressemelding at selskapet mottok advarselsbrevet 5. mars 2026. Selskapet opplyser også at brevet gjelder et inspeksjonsbesøk 7. februar 2025.
Novo forventer å løse saken
Ifølge Novo Nordisk har selskapet siden inspeksjonen jobbet med å håndtere problemene som FDA påpekte under besøket.
Selskapet har fortløpende informert FDA om arbeidet med å forbedre prosedyrene, blant annet gjennom syv tilbakemeldingsrapporter til myndigheten.
Anna Windle, direktør for klinisk utvikling ved Novo Nordisk i USA, uttrykker også tillit til at saken kan løses tilfredsstillende.
Les også
Hun skriver i en pressemelding at Novo Nordisk er trygg på at sakene som er beskrevet i varselbrevet, vil bli håndtert til FDAs fulle tilfredshet.
Saken handler derfor ikke om dokumenterte sikkerhetsproblemer med medisinen, men om hvorvidt rapporteringen av mulige bivirkninger har fulgt gjeldende regelverk.